
化学反应速率是描述化学反应进行快慢的物理量,它对于了解化学反应的本质和规律具有重要意义。本文将通过三步法来探讨化学反应速率的各个方面。

反应速率是指在单位时间内反应物或生成物浓度的变化量。通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。反应速率常以单位为mol/(L·s)或mol/(L·mi)等表示。

反应速率方程是描述反应速率与反应物浓度的关系方程。根据质量作用定律,反应速率与反应物浓度的平方成正比。对于一个简单的反应,反应速率方程可以表示为:
rae = k[C]2
其中,rae表示反应速率,[C]表示反应物浓度,k表示反应速率常数,与反应本身有关。

反应速率常数是描述反应速率与反应物浓度之间关系的常数,它的大小反映了反应的快慢程度。反应速率常数与反应物的性质、温度和压力有关。在一定温度下,反应速率常数可以通过实验测定。

反应速率的计算可以通过测量单位时间内反应物或生成物浓度的变化量来实现。常用的测量方法包括化学滴定法、分光光度法、气相色谱法等。根据测得的数据,可以计算出反应速率常数和反应速率。

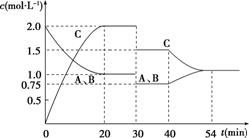
反应速率图解是将反应速率与反应物浓度的关系用图形表示出来。通过图解,可以直观地观察到反应速率与反应物浓度的关系,并判断出反应是否达到平衡状态。常用的图解方法包括速率-浓度图和解速率-时间图。

实验是测定化学反应速率的重要手段之一。通过实验可以测定不同条件下(如不同浓度、不同温度、不同压力等)的反应速率和反应速率常数。实验过程中需要注意控制实验条件,保证实验结果的准确性。常用的实验方法包括化学滴定实验、分光光度实验、气相色谱实验等。
反应速率的测量需要使用专业的测量仪器和设备。常用的测量仪器包括秒表、分光光度计、气相色谱仪等。在测量过程中需要注意仪器的准确性和操作的规范性,以保证测量结果的准确性。同时,也需要对测量结果进行数据处理和分析,以得出可靠的结论。