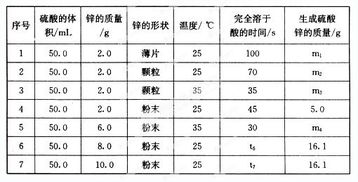
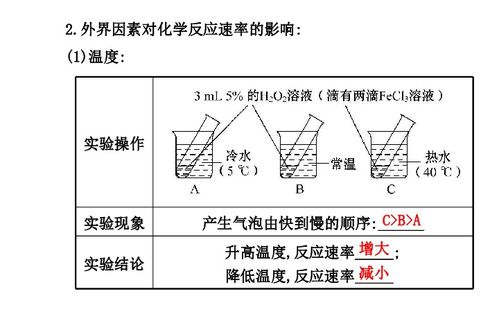
化学反应速率实验是一个通过测量化学反应过程中反应物消耗速率或者产物生成速率来探究反应动力学过程的实验。在这个实验中,我们将采用控制变量法,这是一种科学研究方法,通过保持其他变量不变,只改变一个变量来研究其对实验结果的影响。
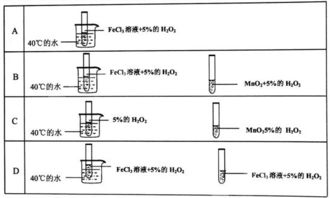
2.1 准备试剂和设备
在进行实验前,我们需要准备好所需的试剂和设备。本实验所需的试剂包括:硫酸、氢氧化钠、醋酸、氯化钠等。设备包括:烧杯、滴定管、恒温水浴、电子天平等。
2.2 设定控制变量
在控制变量法的应用中,我们需要选择一个或多个变量作为实验的变动因素,而其他因素则保持不变。本实验中,我们将控制反应温度为25℃,硫酸和氢氧化钠的反应浓度为0.1M,反应时间为30分钟。
2.3 实施实验
在设定好控制变量后,我们就可以开始进行实验。将反应物在烧杯中混合,然后将混合物转移到恒温水浴中保持温度恒定。在预设的时间间隔(例如:5分钟)内,通过滴定管滴加一定量的反应物,并使用电子天平测量反应物和生成物的质量变化。
2.4 分析数据
实验结束后,我们将收集到一系列关于反应物消耗速率和产物生成速率的数据。通过这些数据,我们可以计算出反应速率常数,以及反应过程中的能量变化等参数。
2.5 结论
通过本次实验,我们得到了控制变量法对化学反应速率的影响数据。这些数据可以用于评估不同因素对化学反应速率的影响程度,并进一步探讨化学反应动力学的基本原理。同时,我们也可以根据这些数据优化实验条件,以提高化学反应的效率和应用范围。
通过本次实验,我们发现控制变量法可以有效控制化学反应的条件,从而实现对化学反应速率的精确控制。在实验过程中,我们观察到了不同因素对化学反应速率的影响规律。例如,当增加反应物的浓度时,化学反应速率会相应增加;而当升高反应温度时,化学反应速率也会提高。这些结果进一步证实了化学反应动力学的基本原理,并为实际生产过程中的化学过程控制提供了重要参考。
我们还发现不同因素对化学反应速率的影响程度存在差异。例如,在本次实验条件下,反应物的浓度对化学反应速率的影响最为显著,其次是反应温度。这些结果提示我们在实际生产过程中可以针对不同因素对化学反应速率的影响程度进行优化调控,以达到提高生产效率和降低能耗的目的。
本次化学反应速率实验通过控制变量法探究了不同因素对化学反应速率的影响规律和影响程度。这些结果有助于我们深入理解化学反应动力学的基本原理,并为实际生产过程中的化学过程控制提供了重要参考。